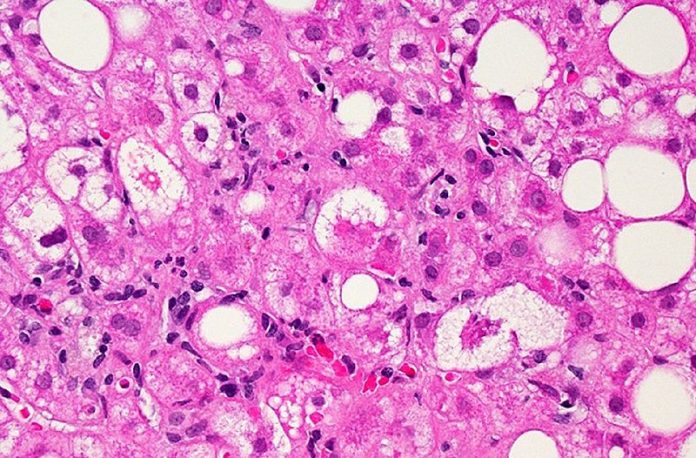
Το Rezdiffra (resmetirom) έχει εγκριθεί από τον FDA των ΗΠΑ για τη θεραπεία ενηλίκων με μη κιρρωτική, μη αλκοολική στεατοηπατίτιδα (NASH) με μέτριες έως προχωρημένες ηπατικές ουλές (ίνωση), για χρήση μαζί με δίαιτα και άσκηση.
Μέχρι τώρα, οι ασθενείς με μη κιρρωτική, μη αλκοολική στεατοηπατίτιδα (NASH) που έχουν επίσης αξιοσημείωτες ουλές στο ήπαρ δεν είχαν φάρμακο που θα μπορούσε να αντιμετωπίσει άμεσα ηπατική βλάβη. FDA's approval of Rezdiffra will, for the first time, provide a treatment option for these patients, in addition to diet and exercise.
NASH is a result of the progression of non-alcoholic fatty συκώτι νόσος όπου συκώτι inflammation, over time, can lead to liver scarring and liver dysfunction. NASH is often associated with other health problems such as high blood pressure and type 2 diabetes. By at least one estimate, approximately 6-8 million people in the U.S. have NASH with moderate to advanced liver scarring, with that number expected to increase.
Το Rezdiffra είναι μερικός ενεργοποιητής ενός υποδοχέα θυρεοειδικών ορμονών. Η ενεργοποίηση αυτού του υποδοχέα από το Rezdiffra στο ήπαρ μειώνει τη συσσώρευση λίπους στο ήπαρ.
Ασφάλεια και αποτελεσματικότητα του Rezdiffra
The safety and efficacy of Rezdiffra was evaluated based on an analysis of a surrogate endpoint at month 12 in a 54-month, randomized, double-blind placebo-controlled trial. The surrogate endpoint measured the extent of συκώτι inflammation and scarring. The sponsor is required to conduct a postapproval study to verify and describe Rezdiffra’s clinical benefit, which will be done through completing the same 54-month study, which is still ongoing. To enroll in the trial, patients needed to have a συκώτι biopsy showing inflammation due to NASH with moderate or advanced συκώτι scarring. In the trial, 888 subjects were randomly assigned to receive one of the following: placebo (294 subjects); 80 milligrams of Rezdiffra (298 subjects); or 100 milligrams of Rezdiffra (296 subjects); once daily, in addition to standard care for NASH, which includes counseling for healthy diet and exercise.
At 12 months, liver biopsies showed that a greater proportion of subjects who were treated with Rezdiffra achieved NASH resolution or an improvement in liver scarring as compared with those who received the placebo. A total of 26% to 27% of subjects who received 80 milligrams of Rezdiffra and 24% to 36% of subjects who received 100 milligrams of Rezdiffra experienced NASH resolution and no worsening of liver scarring, compared to 9% to 13% of those who received placebo and counseling on diet and exercise. The range of responses reflects different pathologists’ readings. In addition, a total of 23% of subjects who received 80 milligrams of Rezdiffra and 24% to 28% of subjects who received 100 milligrams of Rezdiffra experienced an improvement in συκώτι scarring and no worsening of NASH, compared to 13% to 15% of those who received placebo, depending on each pathologist’s readings. Demonstration of these changes in a proportion of patients after just one year of treatment is notable, as the νόσος typically progresses slowly with most patients taking years or even decades to show progression.
Παρενέργειες του Rezdiffra
Οι πιο συχνές ανεπιθύμητες ενέργειες του Rezdiffra περιελάμβαναν διάρροια και ναυτία. Το Rezdiffra συνοδεύεται από ορισμένες προειδοποιήσεις και προφυλάξεις, όπως ηπατική τοξικότητα που προκαλείται από φάρμακα και παρενέργειες που σχετίζονται με τη χοληδόχο κύστη.
Use of Rezdiffra should be avoided in patients with decompensated cirrhosis. Patients should stop using Rezdiffra if they develop signs or symptoms of worsening συκώτι function while on Rezdiffra treatment.
Φαρμακευτικές αλληλεπιδράσεις του Rezdiffra
Η χρήση του Rezdiffra ταυτόχρονα με ορισμένα άλλα φάρμακα, ιδιαίτερα τις στατίνες για τη μείωση της χοληστερόλης, μπορεί να οδηγήσει σε δυνητικά σημαντικές αλληλεπιδράσεις με φάρμακα. Οι πάροχοι υγειονομικής περίθαλψης θα πρέπει να ανατρέξουν στις πλήρεις πληροφορίες συνταγογράφησης για πρόσθετες πληροφορίες σχετικά με αυτές τις δυνητικά σημαντικές φαρμακευτικές αλληλεπιδράσεις με το Rezdiffra, τις συνιστώμενες τροποποιήσεις δοσολογίας και χορήγησης.
Η FDA approved Rezdiffra under the accelerated approval pathway, which allows for earlier approval of drugs that treat serious conditions and address an unmet medical need, based on a surrogate or intermediate clinical endpoint that is reasonably likely to predict clinical benefit. The required aforementioned 54-month study, which is ongoing, will assess clinical benefit after 54 months of Rezdiffra treatment.
Το Rezdiffra έλαβε ονομασίες Breakthrough Therapy, Fast Track και Priority Review για αυτήν την ένδειξη.
Η FDA granted the approval of Rezdiffra to Madrigal Pharmaceuticals.
***
πηγή:
FDA 2024. Δελτίο ειδήσεων – Η FDA εγκρίνει την πρώτη θεραπεία για ασθενείς με ουλές ήπατος λόγω λιπώδους ηπατικής νόσου. Δημοσιεύτηκε 14 Μαρτίου 2024. Διαθέσιμο στο https://www.fda.gov/news-events/press-announcements/fda-approves-first-treatment-patients-liver-scarring-due-fatty-liver-disease
***